Цель работы
Определить экспериментально отношение молярных теплоемкостей газа при постоянном давлении и постоянном объеме и сравнить с теоретическим значением данного отношения, найденным из молекулярно-кинетической теории.
Приборы и принадлежности
Баллон с краном, водяной манометр, компрессор.
Теоретическое введение и описание лабораторной установки
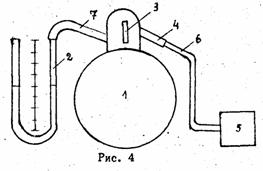
На лабораторной установке (рис. 4) баллон 1 соединен с открытым V-образным водяным манометром 2. Рычажной край 3 через впускной-выпускной штуцер 4 позволяет сообщаться баллону через резиновую трубку 6 с нагнетающим насосом 5 или с атмосферой. В сосуд накачивают воздух до максимально допустимого давления. Через 2-3 мин температура воздуха в сосуде становится равной температуре окружающей среды. Обозначим для первого данного состояния газа его удельный объем V1, давление P1, температуру Т1.
Далее, отсоединив трубку 6 от штуцера 4, быстро нажмем и отпустим рычаг клапана, на мгновение, соединив баллон с окружающим воздухом. Практически сразу давление воздуха в баллоне станет равным атмосферному. Процесс происходит быстро и его можно считать адиабатическим. Новый удельный объем воздуха - V2, давление - P2=P0 (атмосферное) и температура - Т2. Через 2-3 мин воздух в баллоне нагреется до комнатной температуры T3 = Т1, его давление будет P3, а удельный объем V3=V2 (ни масса, ни объем газа не меняются).
Переход из первого, состояния во второе (адиабатический процесс) описывается уравнением Пуассона
![]()
где ![]()
Сравнивая конечное, третье состояние газа с первым, видим, что температура газа в этих состояниях одинакова, следовательно, к этому переходу применим закон Бойля-Мариотта
P1V1=P2V2, (27)
Решая систему двух уравнений ((26), (27)), можно определить γ. Для этого возведем второе уравнение в степень γ разделим его на первое уравнение:
![]()
Так как V2=V3, то ![]() или
или 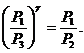
Логарифмируя последнее выражение, получим
![]()
![]()
Обозначим разность уровней жидкости в манометре в первом состоянии h1, а в третьем состоянии - h3. Тогда
P1=P0+h1, P3=P0+h3, (P2=P0)
Подставим значения Р1, Р2, Р3 в соотношение (28):
![]()
В данном случае h1 и h3 намного меньше Р0, поэтому отношение разности логарифмов можно заменить отношением разности чисел, т.е.
![]()
Это дает расчетную формулу для нашего опыта
![]()
В молекулярно-кинетической теории молярные теплоемкости газа Сp и Сv определяются через число степеней свобода молекулы i и универсальную газовую постоянную R :
![]()
Найдем их отношение
![]()
В данном случае воздух не очищается от влаги и содержит большое количество паров воды, поэтому число степеней свободы будет соответствовать трехатомным молекулам, т.е. i = 6.
 Вблизи поверхности Земли ускорение свободного падения зависит ОТ широты местности. Это объясняется нешарообразностью формы Земли и влиянием суточного вращения Земли вокруг своей оси.
Вблизи поверхности Земли ускорение свободного падения зависит ОТ широты местности. Это объясняется нешарообразностью формы Земли и влиянием суточного вращения Земли вокруг своей оси.
 Законы физики основаны на фактах, установленных опытным путем.
Законы физики основаны на фактах, установленных опытным путем.
 Турбина 16 века использовавшая энергию движущейся воды, применялась для привода ирригационных насосов.
Турбина 16 века использовавшая энергию движущейся воды, применялась для привода ирригационных насосов.